Las necesidades médicas no cubiertas en el I+D farmacéutico
- Eupati
- 28/11/2022
- Actualización: 30/11/2022
- Eupati
- 28/11/2022
- Actualización: 30/11/2022

La práctica clínica ha avanzado históricamente gracias a la investigación, al pensamiento crítico y fundamentalmente al diálogo entre las diferentes partes involucradas, entre los que se encuentra la sociedad y los pacientes.
1) Validar lo que precisa la población, en general, y los pacientes en particular.
2) Comprender el impacto que tendría la llegada de un nuevo tratamiento.
Nuestras entradas

La Agencia Europea del Medicamento (EMA) define los PROs como los resultados de salud que los pacientes reportan sobre sus enfermedades y tratamientos. Y hace hincapié en dos…

Las agencias reguladoras velan por la protección y promoción de la salud en nuestra sociedad. La de Estados Unidos es la FDA, la europea la EMA y la española la AEMPS. Y entre sus…
Contacta con nosotros
01
VISITA EL TOOL BOX DE EUPATI
¿Qué es una necesidad médica
no cubierta?
La regulación europea, según lo establecido en el 2º párrafo del artículo 4 del reglamento Nº. 507/2006, especifica que podemos hablar de necesidad médica no cubierta cuando:
“Carecemos de un método satisfactorio de diagnóstico, prevención o tratamiento o, aun existiendo alguno, que el nuevo medicamento suponga una ventaja terapéutica importante para los afectados”
Aunque nos encontramos con los siguientes inconvenientes:
- No concreta qué es una ventaja importante.
No hay guías específicas que ayuden a aclararlo.
Lo que ha terminado generando que las compañías, reguladores, evaluadores, pacientes y pagadores actúen en base a sus propias definiciones, como recogió Jordi Llinares en su presentación “Necesidades médicas insatisfechas: una introducción a las definiciones y percepciones de las partes interesadas” en la reunión de la EMA con la comunidad de pagadores de junio de 2019. En concreto, Llinares señaló cómo una búsqueda bibliográfica identificó hasta 16 definiciones de necesidad médica no cubierta. Aunque, en un ejercicio integrador después de repasar la importancia de este concepto, concluyó que futuras definiciones deberían recoger de alguna forma, la severidad o carga de la enfermedad y no solo la actual disponibilidad de tratamientos. Aunque, en este sentido, declaraba recientemente EFPIA, la patronal europea de la industria farmacéutica, que corremos el riesgo de perdernos terapias importantes para los pacientes si acotamos el término y limitamos los incentivos a los tratamientos que únicamente se ajusten a una definición concreta de necesidad médica.
01
¿Qué es una necesidad médica no cubierta?
¿Qué es una necesidad médica no cubierta?
La regulación europea, según lo establecido en el 2º párrafo del artículo 4 del reglamento Nº. 507/2006, especifica que podemos hablar de necesidad médica no cubierta cuando:
“Carecemos de un método satisfactorio de diagnóstico, prevención o tratamiento o, aun existiendo alguno, que el nuevo medicamento suponga una ventaja terapéutica importante para los afectados”
Aunque nos encontramos con los siguientes inconvenientes:
- No concreta qué es una ventaja importante.
No hay guías específicas que ayuden a aclararlo.
Lo que ha terminado generando que las compañías, reguladores, evaluadores, pacientes y pagadores actúen en base a sus propias definiciones, como recogió Jordi Llinares en su presentación “Necesidades médicas insatisfechas: una introducción a las definiciones y percepciones de las partes interesadas” en la reunión de la EMA con la comunidad de pagadores de junio de 2019. En concreto, Llinares señaló cómo una búsqueda bibliográfica identificó hasta 16 definiciones de necesidad médica no cubierta. Aunque, en un ejercicio integrador después de repasar la importancia de este concepto, concluyó que futuras definiciones deberían recoger de alguna forma, la severidad o carga de la enfermedad y no solo la actual disponibilidad de tratamientos. Aunque, en este sentido, declaraba recientemente EFPIA, la patronal europea de la industria farmacéutica, que corremos el riesgo de perdernos terapias importantes para los pacientes si acotamos el término y limitamos los incentivos a los tratamientos que únicamente se ajusten a una definición concreta de necesidad médica.
Este escenario es razón más que suficiente para que sigamos dialogando hasta encontrar un mejor enfoque. De hecho, creemos que una buena definición de necesidad médica no cubierta podría acelerar la llegada de medicamentos esenciales para un grupo –o subgrupo– de pacientes que lo espera, así como evitar que aparezcan productos que incumplan nuestras expectativas. En esta línea, la Comisión Europea anunció en 2020 su intención de llevar a cabo una importante revisión de la legislación farmacéutica de la UE, incluyendo cambios en su planteamiento para abordarlas. La consulta estuvo abierta al público hasta diciembre del 2021 y añadía, a su vez, otras dimensiones a considerar en la ecuación, como, por ejemplo, la accesibilidad de los medicamentos y la sostenibilidad de los sistemas sanitarios.

Este escenario es razón más que suficiente para que sigamos dialogando hasta encontrar un mejor enfoque. De hecho, creemos que una buena definición de necesidad médica no cubierta podría acelerar la llegada de medicamentos esenciales para un grupo –o subgrupo– de pacientes que lo espera, así como evitar que aparezcan productos que incumplan nuestras expectativas. En esta línea, la Comisión Europea anunció en 2020 su intención de llevar a cabo una importante revisión de la legislación farmacéutica de la UE, incluyendo cambios en su planteamiento para abordarlas. La consulta estuvo abierta al público hasta diciembre del 2021 y añadía, a su vez, otras dimensiones a considerar en la ecuación, como, por ejemplo, la accesibilidad de los medicamentos y la sostenibilidad de los sistemas sanitarios.

La iniciativa PREFER, a su vez, está publicando análisis sobre lo que piensan los pacientes de diferentes patologías: hemofilia, mieloma, cáncer de pulmón, artritis reumatoide, etc. Puedes comenzar preguntándote si estás de acuerdo con esos resultados y si cambiarían en población española.
ESCENARIOS
A día de hoy podemos afirmar que las necesidades no cubiertas constituyen un pilar estratégico para la Unión Europea. Prueba de ello es que son un criterio para la evaluación acelerada, la autorización condicional o para entrar en el listado de medicamentos prioritarios de la EMA (Prime).
“Los medicamentos huérfanos y pediátricos cumplen por definición los criterios de necesidad médica no cubierta”
No obstante, existen diferentes escenarios en los que podríamos identificar una necesidad médica no cubierta. Por ejemplo, cuando:
1) Carecemos de tratamientos adecuados para abordar una enfermedad determinada, el caso más común sería el de las enfermedades raras.
2) Los medicamentos actuales no resuelven la problemática de todo el colectivo, como puede ocurrir en el cáncer.
3) El arsenal terapéutico no es útil para para resolver cada situación dentro de un colectivo de pacientes, aunque la mayoría se pueda estar beneficiando, como ocurre las enfermedades inmunomediadas. En estos casos, entendemos que nos podríamos encontrar con pacientes doblemente excluidos. Primero, porque no se benefician de los tratamientos actuales, independientemente de la naturaleza del motivo que lo cause: falta de eficacia, reacciones adversas, etc. Y, segundo, porque también les resultaría más y más difícil recibir nuevos tratamientos según se vayan cubriendo las necesidades de su colectivo.
02
ESCENARIOS
03
LA PROPUESTA
LA PROPUESTA
La clave para continuar impulsando el progreso y, no excluir a nadie que se encuentre en los diferentes escenarios, radicará en la flexibilidad con la que actuemos. Sin embargo, la única recomendación directa que hemos encontrado es que debemos continuar examinando estos puntos de vista. Sobre todo, porque, para los pacientes que no pueden beneficiarse de la medicina actual, sus casos, siempre deberían considerarse como no resueltosUn modelo integrador para identificar necesidades no cubiertas debe dividir los elementos a considerar en 3 categorías:
1) La disponibilidad de tratamientos alternativos.
2) Gravedad o carga de la enfermedad.
3) El tamaño de la población afectada. Si bien, parece haber unanimidad a la hora de restar peso a este tercer apartado.
01
VISITA EL TOOL BOX DE EUPATI
1) carecemos de tratamientos adecuados para abordar una enfermedad determinada, el caso más común sería el de las enfermedades raras.
2) los medicamentos actuales no resuelven la problemática de todo el colectivo, como puede ocurrir en el cáncer.
3) el arsenal terapéutico no es útil para para resolver cada situación dentro de un colectivo de pacientes, aunque la mayoría se pueda estar beneficiando, como ocurre las enfermedades inmunomediadas. En estos casos, entendemos que nos podríamos encontrar con pacientes doblemente excluidos. Primero, porque no se benefician de los tratamientos actuales, independientemente de la naturaleza del motivo que lo cause: falta de eficacia, reacciones adversas, etc. Y, segundo, porque también les resultaría más y más difícil recibir nuevos tratamientos según se vayan cubriendo las necesidades de su colectivo.
ESCENARIOS
De momento, se puede afirmar que las necesidades no cubiertas se han convertido en un pilar estratégico para la Unión Europea. A día de hoy, son un requisito de elegibilidad para la evaluación acelerada, la autorización condicional y un criterio para elaborar el listado de medicamentos prioritarios de la EMA (European Medicines Agency).
No obstante, existen diferentes escenarios en los que podríamos identificar una necesidad médica no cubierta. Por ejemplo, cuando:
1) carecemos de tratamientos adecuados para abordar una enfermedad determinada, el caso más común sería el de las enfermedades raras;
2) los medicamentos actuales no resuelven la problemática de todo el colectivo, como puede ocurrir en el cáncer;
3) el arsenal terapéutico no es útil para para resolver cada situación dentro de un colectivo de pacientes. Independientemente de que la mayoría se pueda estar beneficiando, como podría ocurrir en las enfermedades inmunomediadas.

02
VISITA EL TOOL BOX DE EUPATI
escenarios
A día de hoy podemos afirmar que las necesidades no cubiertas constituyen un pilar estratégico para la Unión Europea. Prueba de ello es que son un criterio para la evaluación acelerada, la autorización condicional o para entrar en el listado de medicamentos prioritarios de la EMA (Prime).
“Los medicamentos huérfanos y pediátricos cumplen por definición los criterios de necesidad médica no cubierta”
No obstante, existen diferentes escenarios en los que podríamos identificar una necesidad médica no cubierta. Por ejemplo, cuando:
1) Carecemos de tratamientos adecuados para abordar una enfermedad determinada, el caso más común sería el de las enfermedades raras.
2) Los medicamentos actuales no resuelven la problemática de todo el colectivo, como puede ocurrir en el cáncer.
3) El arsenal terapéutico no es útil para para resolver cada situación dentro de un colectivo de pacientes, aunque la mayoría se pueda estar beneficiando, como ocurre las enfermedades inmunomediadas. En estos casos, entendemos que nos podríamos encontrar con pacientes doblemente excluidos. Primero, porque no se benefician de los tratamientos actuales, independientemente de la naturaleza del motivo que lo cause: falta de eficacia, reacciones adversas, etc. Y, segundo, porque también les resultaría más y más difícil recibir nuevos tratamientos según se vayan cubriendo las necesidades de su colectivo.

03
VISITA EL TOOL BOX DE EUPATI
la propuesta
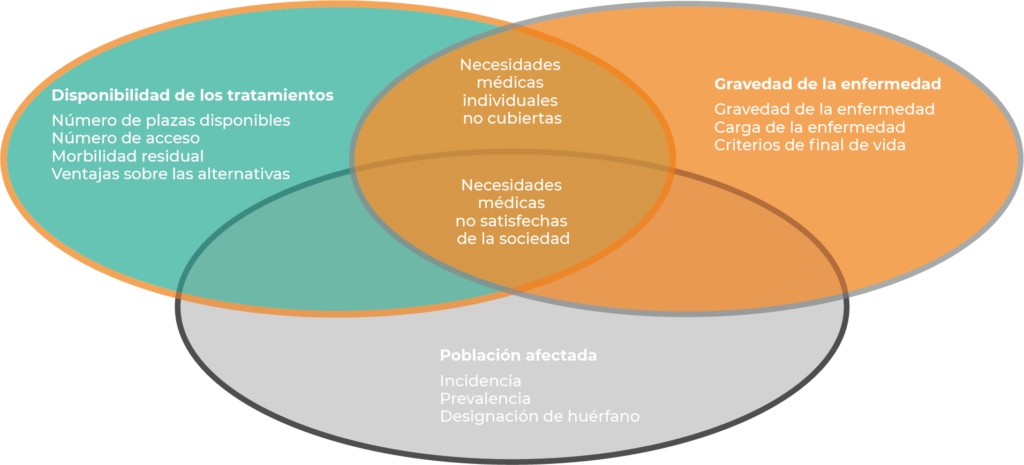
La clave para continuar impulsando el progreso y, no excluir a nadie que se encuentre en los diferentes escenarios, radicará en la flexibilidad con la que actuemos. Sin embargo, la única recomendación directa que hemos encontrado es que debemos continuar examinando estos puntos de vista. Sobre todo, porque, para los pacientes que no pueden beneficiarse de la medicina actual, sus casos, siempre deberían considerarse como no resueltosUn modelo integrador para identificar necesidades no cubiertas debe dividir los elementos a considerar en 3 categorías:
1) La disponibilidad de tratamientos alternativos.
2) Gravedad o carga de la enfermedad.
3) El tamaño de la población afectada. Si bien, parece haber unanimidad a la hora de restar peso a este tercer apartado.
04
VISITA EL TOOL BOX DE EUPATI
La opinión de los pacientes importa
Las agencias reguladoras se están acercando a esta visión integradora. En concreto, cuando autorizan medicamentos en función de elementos que van más allá de la mera disponibilidad de tratamientos alternativos adecuados. Un hecho que se evidencia con los mecanismos de consulta a los pacientes que se han diseñado -antes de tomar una decisión- con el fin comprender el impacto de las enfermedades en la vida de las personas na participación recogida en la legislación europea y que se está extendiendo a las políticas nacionales de los estados miembros de la Unión Europea, aunque no en todos por igual.
Por otro lado, un estudio reveló cómo las necesidades no cubiertas en oncología se siguen argumentando con frecuencia, incluso cuando existen alternativas de tratamiento con expectativas de supervivencia relativamente alentadoras. Si bien, los investigadores señalan que es una práctica que aún debe estandarizarse.

05
VISITA EL TOOL BOX DE EUPATI
el reto
El principal reto al que nos enfrentamos es el de garantizar un marco normativo que apoye la innovación para los casos más graves y urgentes, y que, al mismo tiempo, ofrezca también garantías suficientes a la hora de cubrir soluciones específicas.
Si quieres consultar el rol que desempeñan los representantes de los pacientes en los comités de la EMA te recomendamos visitar el siguiente documento:

Desde Eupati-España añadimos la importancia de seguir potenciando las asociaciones de pacientes para que puedan transmitir de manera significativa el sentir de sus colectivos, independientemente de su tamaño, recursos y prevalencia de la patología que representan.

La iniciativa PREFER, a su vez, está publicando análisis sobre lo que piensan los pacientes de diferentes patologías: hemofilia, mieloma, cáncer de pulmón, artritis reumatoide, etc. Puedes comenzar preguntándote si estás de acuerdo con esos resultados y si cambiarían en población española.
La opinión de los pacientes importa
Las agencias reguladoras se están acercando a esta visión integradora. En concreto, cuando autorizan medicamentos en función de elementos que van más allá de la mera disponibilidad de tratamientos alternativos adecuados. Un hecho que se evidencia con los mecanismos de consulta a los pacientes que se han diseñado -antes de tomar una decisión- con el fin comprender el impacto de las enfermedades en la vida de las personas na participación recogida en la legislación europea y que se está extendiendo a las políticas nacionales de los estados miembros de la Unión Europea, aunque no en todos por igual.
Por otro lado, un estudio reveló cómo las necesidades no cubiertas en oncología se siguen argumentando con frecuencia, incluso cuando existen alternativas de tratamiento con expectativas de supervivencia relativamente alentadoras. Si bien, los investigadores señalan que es una práctica que aún debe estandarizarse.
04
La opinión de los pacientes importa
05
EL RETO
EL RETO
El principal reto al que nos enfrentamos es el de garantizar un marco normativo que apoye la innovación para los casos más graves y urgentes, y que, al mismo tiempo, ofrezca también garantías suficientes a la hora de cubrir soluciones específicas.
Si quieres consultar el rol que desempeñan los representantes de los pacientes en los comités de la EMA te recomendamos visitar el siguiente documento:
Desde Eupati- España añadimos la importancia de seguir potenciando las asociaciones de pacientes para que puedan transmitir de manera significativa el sentir de sus colectivos, independientemente de su tamaño, recursos y prevalencia de la patología que representan.

REFERENCIAS
Kohl S. (2021). Putting the patient at the centre – Pharmaceutical Strategy for Europe welcomed by hospital pharmacists. European journal of hospital pharmacy: science and practice, 28(1), 54–56. https://doi.org/10.1136/ejhpharm-2020-002629
Vennemann, M., Ruland, V., Kruse, J. P., Harloff, C., Trübel, H., & Gielen-Haertwig, H. (2019). Future unmet medical need as a guiding principle for pharmaceutical R&D. Drug discovery today, 24(9), 1924–1929. https://doi.org/10.1016/j.drudis.2019.06.004
https://www.ema.europa.eu/en/documents/presentation/presentation-unmet-medical-need-introduction-definitions-stakeholder-perceptions-jllinares-garcia_en.pdf
https://www.efpia.eu/about-medicines/development-of-medicines/unmet-medical-need/
Horgan, D., Borisch, B., Eliasen, B., Kapitein, P., Biankin, A. V., Gijssels, S., Zaiac, M., Fandel, M. H., Lal, J. A., Kozaric, M., Moss, B., De Maria, R., Geanta, M., Nowak, F., Montserrat-Moliner, A., & Riess, O. (2022). Meeting the Need for a Discussion of Unmet Medical Need. Healthcare (Basel, Switzerland), 10(8), 1578. https://doi.org/10.3390/healthcare10081578
https://www.ema.europa.eu/en/documents/presentation/presentation-unmet-medical-need-j-llinares-ema_en.pdf
Vreman, R. A., Heikkinen, I., Schuurman, A., Sapede, C., Garcia, J. L., Hedberg, N., Athanasiou, D., Grueger, J., Leufkens, H., & Goettsch, W. G. (2019). Unmet Medical Need: An Introduction to Definitions and Stakeholder Perceptions. Value in health : the journal of the International Society for Pharmacoeconomics and Outcomes Research, 22(11), 1275–1282 https://doi.org/10.1016/j.jval.2019.07.007
Lu, E., Shatzel, J., Shin, F., & Prasad, V. (2017). What constitutes an «unmet medical need» in oncology? An empirical evaluation of author usage in the biomedical literature. Seminars in oncology, 44(1), 8–12. https://doi.org/10.1053/j.seminoncol.2017.02.009
Horgan, D., Spanic, T., Apostolidis, K., Curigliano, G., Chorostowska-Wynimko, J., Dauben, H. P., Lal, J. A., Dziadziuszko, R., Mayer-Nicolai, C., Kozaric, M., Jönsson, B., Gutierrez-Ibarluzea, I., Fandel, M. H., & Lopert, R. (2022). Towards Better Pharmaceutical Provision in Europe-Who Decides the Future?. Healthcare (Basel, Switzerland), 10(8), 1594. https://doi.org/10.3390/healthcare10081594
Wang T, McAuslane N, Goettsch WG, Leufkens HGM, De Bruin ML. Challenges and Opportunities for Companies to Build HTA/Payer Perspectives Into Drug Development Through the Use of a Dynamic Target Product Profile. Front Pharmacol. 2022 Jul 18;13:948161. doi: 10.3389/fphar.2022.948161. PMID: 35924050; PMCID: PMC9340272.
Haerry, D., Landgraf, C., Warner, K., Hunter, A., Klingmann, I., May, M., & See, W. (2018). EUPATI and Patients in Medicines Research and Development: Guidance for Patient Involvement in Regulatory Processes. Frontiers in medicine, 5, 230. https://doi.org/10.3389/fmed.2018.00230
Nuestras entradas

La Agencia Europea del Medicamento (EMA) define los PROs como los resultados de salud que los pacientes reportan sobre sus enfermedades y tratamientos. Y hace hincapié en dos…

Las agencias reguladoras velan por la protección y promoción de la salud en nuestra sociedad. La de Estados Unidos es la FDA, la europea la EMA y la española la AEMPS. Y entre sus…